淋巴细胞的B系或T系细胞在骨髓内异常增生而导致的恶性肿瘤--急性淋巴细胞白血病(ALL)是一种比较少见的疾病,它在成人群体中,只占了所有白血病病例的15%,这种疾病的预后非常差,一般中位总生存期只有3-6个月。只有少于50%的患者在接受了常见的化疗治疗手段后产生应答。
复发或难治性ALL的成人患者的5年总生存率也非常低,不到10%。所以该疾病需要更多新型且有效的治疗方案。去年六月,欧盟委员会对Besponsa的批准让该领域走出了重要的一步,它为那些复发或难治性的白血病患者提供了除化疗外的新治疗方案。
Besponsa(inotuzumab ozogamicin)被欧盟批准用于单药治疗复发或难治性的CD22+成人B细胞前体急性淋巴细胞白血病(ALL),而且这些ALL患者在接受Besponsa之前都接受过至少一种TKI激酶抑制剂治疗。它也是欧盟批准的第一个用于以上适应症的抗体偶联药物(ADC)。
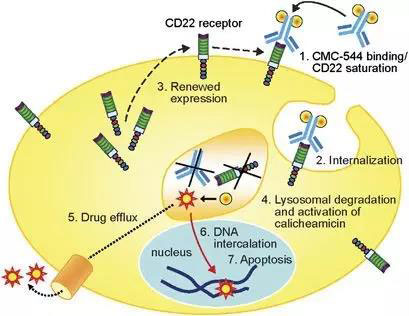
辉瑞的Besponsa是一款充满潜力的新疗法,它作为一种创新的抗体药物偶联物,由两部分组成。它是由靶向CD22的单克隆抗体inotuzumab与细胞毒制剂卡奇霉素(calicheamicin)偶联而成。CD22是在癌细胞上发现的一种细胞表面抗原,存在于几乎所有的B-ALL患者中,也因此该药物能够靶向癌细胞,并与之表面的CD22抗原结合,接着卡奇霉素会发挥它的功效,摧毁了癌细胞。
这是一种致命的罕见疾病,如果治疗不及时的话,患者会在短短几个月里失去生命。Besponsa的批准对于复发性或难治性B细胞急性淋巴性白血病的成人患者来说,是一种新疗法,也帮助很多患者解决了重大的需求,让更多的患者坚持到进行干细胞移植的那一刻。
详情用药请扫描下方二维码,获取更多药品说明书、药品价格、药品副作用、服用方法等资讯。