Kymriah(tisagenlecleucel,CTL019)
作者:admin 时间:2018-10-19 17:10
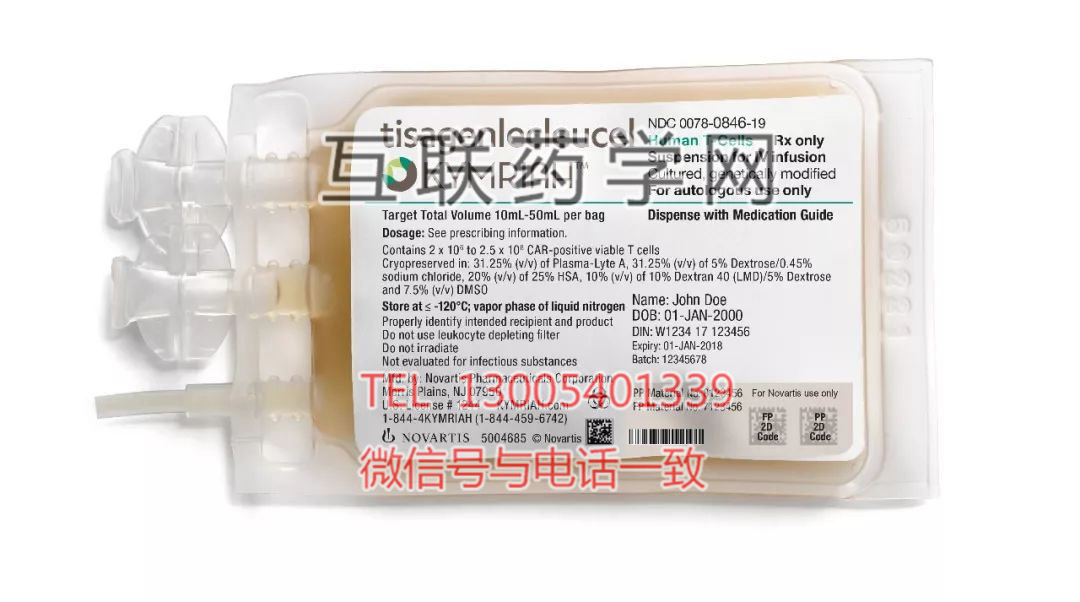
Kymriah(tisagenlecleucel,CTL019)在2017年8月份获得批准上市,用于治疗复发或难治性B细胞急性淋巴细胞白血病(RR ALL)的儿童和25岁以下年轻成人患者。
持续研究对75名输注超过3个月的患者进行随访分析,以追踪Kymriah的可持续性和长期安全性。其中,中位数超过1年的随访患者的总体反应率为81%(95%CI:71%至89%)。所有患者在60%的患者中达到完全缓解(CR),21%的患者达到CR,但未恢复全血细胞计数指数(CRI),所有患者均在[5861] 28微残留病(MRD)(未发现95%)。中位随访期为13.1个月。
达到CR CRi的患者未达到中位缓解期。缓解期保持很长一段时间,存活率在6个月时没有复发80%。中位无事件生存率为6个月(95%CI:60%-82%),12个月:小时(95%CI 35%-64%)为50%,无事件生存率为73%它不符合。输血患者6个月的75年总生存率在12个月内为90%(95%CI:81%至95%),76%(63% - 86%95%CI)。
在接受输入长达20个月的患者中检测到Kymriah细胞。 Kimuria的中位数为168天(持续范围:20至617天,n = CR CRi患者60人)。所有患者均表现出B细胞发育不良(缓解的细胞数量少于或少于B细胞数量),但这种效应Kymriah可用于治疗目的。
Kymriah(tisagenlecleucel,CTL019)最常见的非血液学不良事件是细胞因子释放综合征(CRS,77%),发热(40%)和食欲不振(39%)。致热性中性粒细胞减少症(36%),头痛(36%)。 73%的患者经历了34级治疗相关的AE。 CRS发生在77%的患者中,并且是一种称为可在患者体内激活的细胞的并发症。只有通过可用于保护患者安全的治疗中心网络进行认证,这些中心才能完全接受使用Kymriah和适当患者护理的培训。
注:药品如有新包装,以新包装为准。以上资讯仅供医护人员内部讨论,不作任何用药依据,具体用药指引,请咨询主治医师。
更多用药详情请扫描下方二维码,获取更多药品说明书、药品价格、药品副作用、服用方法等资讯。

本文链接地址:http://www.hulianmedical.com//a/xinteyaopin/xueyeke/2018/1019/1279.html,如需转载,烦请注明出自互医网络科技 http://www.hulianmedical.com。谢谢!
上一篇:hemlibra
下一篇:Venclexta/Venclyxto

 Kymriah(tisagenlecleucel,CTL019)
Kymriah(tisagenlecleucel,CTL019) Primovir(奈玛特韦利托那韦
Primovir(奈玛特韦利托那韦 抗病毒治疗新冠肺炎特效
抗病毒治疗新冠肺炎特效 Paracetamol(扑热息痛)中文
Paracetamol(扑热息痛)中文 KRYSTEXXA(pegloticase injection,
KRYSTEXXA(pegloticase injection, 安琪坦(Utrogestan)中文说
安琪坦(Utrogestan)中文说 抗生素非达霉素DIFICLIR(f
抗生素非达霉素DIFICLIR(f 依普利酮Inspra(Eplerenone)
依普利酮Inspra(Eplerenone) 那他霉素natamet滴眼液中文
那他霉素natamet滴眼液中文